基本定律
热力学是具有严谨的理论体系的少数几门学科之一,它是以带有公理性质的四个基本定律为基础,其中第一定律和第二定律尤为重要。热力学基本定律确定了描述体系性质的状态变量及其关系。热力学第0定律从热平衡出发引入了称为温度T的状态变量。第一定律引入了内能U状态变量,确定了内能与热和功之间的能量守恒关系。第二定律引入了熵S状态变量,提出了自发过程发生方向的判据。第三定律为计算熵的绝对值提供了参考状态。
前面已提及的体积V和压力p也是体系的状态变量,由于它们在力学中已有明确的定义,且力学又形成于热力学之先,所以在热力学中不必用专门的定律定义它们了。另外,为了处理在不同条件下各种类型的热力学问题方便起见,在上述基本定律基础上,又引入了焓H、功函F和自由能G等状态变量,从而使热力学成为完整的理论体系,可以采用演绎方式解决要研究的问题。
前面已提及的体积V和压力p也是体系的状态变量,由于它们在力学中已有明确的定义,且力学又形成于热力学之先,所以在热力学中不必用专门的定律定义它们了。另外,为了处理在不同条件下各种类型的热力学问题方便起见,在上述基本定律基础上,又引入了焓H、功函F和自由能G等状态变量,从而使热力学成为完整的理论体系,可以采用演绎方式解决要研究的问题。
教育新鲜事
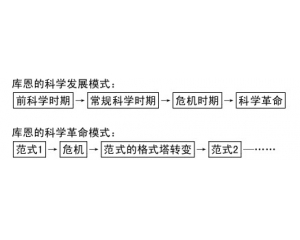 “复式”化学革命模式
“复式”化学革命模式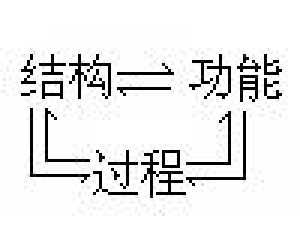 结构、过程与功能的相互
结构、过程与功能的相互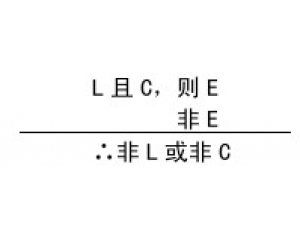 检验的复杂性
检验的复杂性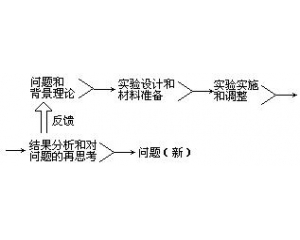 实验操作的程序
实验操作的程序