航天器里的水源和电源―氢氧燃料电池
自从1957年10月4日原苏联发射了第一颗人造地球卫星、人类进入“太空时代”以来,现在已有2000多人乘坐宇宙飞船巡天揽月、遨 0 太空。对此,人们不禁要问:远离地球的飞船内部所用的电能从何而来?宇航员所需用的水又是怎样解决的?如果从地球上带着蓄电池和水上天,自然会加大飞船的重量,这不是上策。为此,科学家们想到了氢氧燃料电池,因为它既可解决电能问题,又可解决宇航员的饮水问题,真是兼而有之,一举两得!所谓燃料电池是电燃料(氢、肼、烃、甲醇、液氨、煤气、天然气等)、氧化剂(氧气、空气、氯、溴等)、电极(多孔烧结镍电极、多孔银电极等)和电解质(氢氧化钾溶液或固体电解质——含有二氧化锆和其他氧化物的陶瓷)组成的。利用燃料和氧化剂之间的氧化—还原反应,可以从化学能直接产生电能,从而大大提高能量的转换率。
当前广泛应用于航天飞行的是氢氧燃料电池。在这种电池中,阳极碳电极的表面嵌有细微分散的铂或钯粒子作催化剂,氢气通过极上的细微空隙进行扩散;阳极上氧气通过浸有氧化钴、铂或银为催化剂的一个多孔碳电极进行扩散。阳极和阴极用一种电解质(如氢氧化钠或氢氧化钾溶液)分隔开。氢通过阳极扩散,以氢原子的形式被吸附在电极的表面上,它同电解质溶液中的氢氧根离子反应生成水。在阳极产生的电子通过外电路流到阴极。通过阴极扩散的氧气被吸附在电极表面,在这里被还原为氢氧根离子。氢氧根离子从氧电极(阴极)经电解质溶液迁移到氢电极(阳极),从而完成一个循环。
美国已在曼哈顿地区建成了一座4800千瓦的燃料电池发电站。另外,氢氧燃料电池的一个重要特点是从太阳捕获动力。利用现代的催化方法可以用太阳光将水分解为氢气和氧气,然后将它们应用于燃料电池中产生电能。据预测,到下一个世纪,燃料电池将成为一颗新的熠熠发光的“电星”,造福于人类。
当前广泛应用于航天飞行的是氢氧燃料电池。在这种电池中,阳极碳电极的表面嵌有细微分散的铂或钯粒子作催化剂,氢气通过极上的细微空隙进行扩散;阳极上氧气通过浸有氧化钴、铂或银为催化剂的一个多孔碳电极进行扩散。阳极和阴极用一种电解质(如氢氧化钠或氢氧化钾溶液)分隔开。氢通过阳极扩散,以氢原子的形式被吸附在电极的表面上,它同电解质溶液中的氢氧根离子反应生成水。在阳极产生的电子通过外电路流到阴极。通过阴极扩散的氧气被吸附在电极表面,在这里被还原为氢氧根离子。氢氧根离子从氧电极(阴极)经电解质溶液迁移到氢电极(阳极),从而完成一个循环。

美国已在曼哈顿地区建成了一座4800千瓦的燃料电池发电站。另外,氢氧燃料电池的一个重要特点是从太阳捕获动力。利用现代的催化方法可以用太阳光将水分解为氢气和氧气,然后将它们应用于燃料电池中产生电能。据预测,到下一个世纪,燃料电池将成为一颗新的熠熠发光的“电星”,造福于人类。
相关文章
教育新鲜事
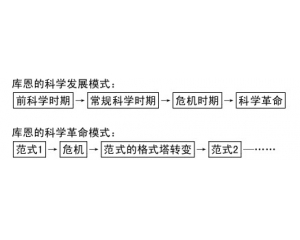 “复式”化学革命模式
“复式”化学革命模式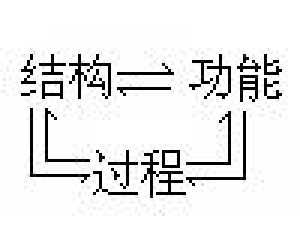 结构、过程与功能的相互
结构、过程与功能的相互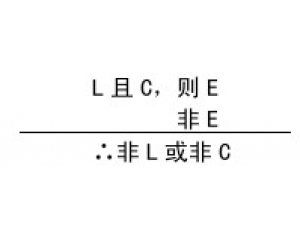 检验的复杂性
检验的复杂性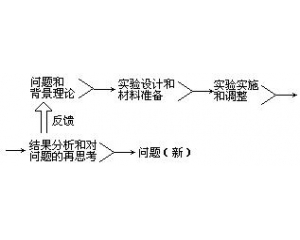 实验操作的程序
实验操作的程序