���л�ѧԭ��ع���ԭ��
1�����弰��ӳʵ��
�ѻ�е��ת��Ϊ����ܵ��豸����ʵ���Ƿ�����������ԭ��Ӧ��
2����ɱ�
(1)��2����Ծ�Բ�һ���Ľ����缫(�ձ�Ϊ�������ϻ�ߴ�ʯī)��
(2)�������缫����������Һ�С�
(3)�������缫����ɺϱտ��ƻ�·(�������缫�����������������)��
(4)���Է��Է���������ԭ��Ӧ��
3��ԭ��
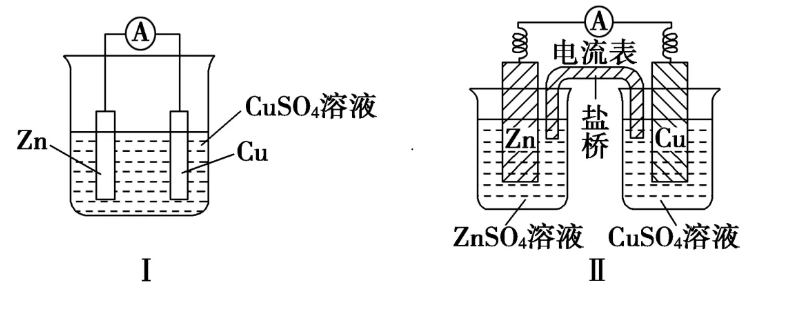
��ͼ��Cu--Znԭ���
(1)��ӳ����ԭ��
(2)ԭ����е�������λ
������������λ���Ӹ����ų��������ע��������
������������������������븺����
�������ӵ�ת�Ʒ�λ���������Һ�У���������ת�ƣ�������������ת�ơ�
(3)�����豸�Ľ�Ϊ
ͼ����Zn��CuSO4ˮ��Һ����������Cu2��������һ����Zn��Cu2��������ӳ�����豸�о��л�е�ܺ͵���ܵ�ת��������һ���ֻ�е��ת��������Դ���豸�ĜضȻ�������
ͼ����Zn��CuSO4ˮ��Һ������2�����Zn��Cu2���������������Ҳ���Zn��Cu2��������ӳ��ȫ���̣���˽��ǻ�е��ת�����˵���ܣ�������ƽ�ȣ����ӳ�ʱ�䳤��
(4)���Ź�Ч
�������ڵ�·�������ϱտ��ƻ�·��
�����⸺��ɣ�ʹԭ��س�����ɵ�������
������
1��ԭ��ص�ԭ��ʾ��ͼ
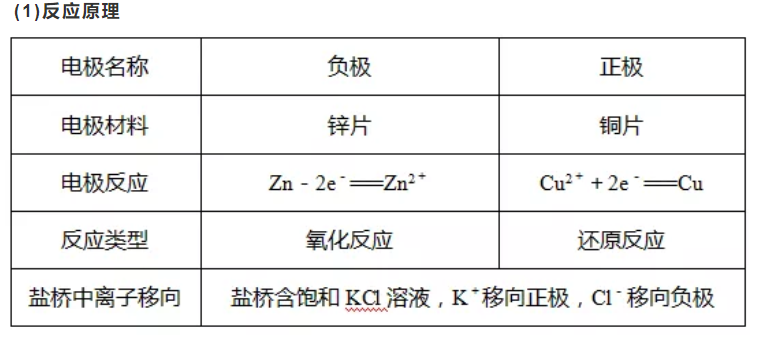
���⣺
��һ�㸺���������ϽϿ��ʣ������������ϻ�ǽ������ϲ����ʡ�
��һ�㸺���ڽ��Ʒ�ʻ��⣬���������ݻ�Ʒ���������ӡ�
���������ţ������е���������������������������������
2��ԭ��ص��жϷ�ʽ
(1)��������û�����õ�Դ�������õ�Դ��Ϊ���أ������õ�Դ�Ľ���Ϊԭ��ء�
(2)������ԭ��صIJ������ж��豸�Dz���Ϊԭ��أ���ʽ���£�
(3)�����ӣ��������õ�Դʱ�������濪���Բ��ϴ��һ��Ϊԭ��أ���ĸ��ؿɿ������ء�
3��ԭ������������жϵ����ַ�ʽ
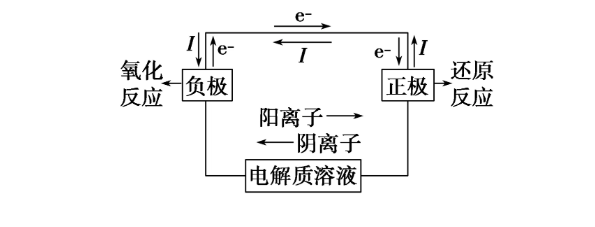
(1)�ɹ���ԭ��ص�������ԭ�����жϡ�
һ������ԽϿ��ʵĽ�������Ϊ����������Բ����ʵĽ������ϻ��ܵ����Եķǽ�������Ϊ������
(��Ҳ��һЩ�������뿪����һ�£���Mg��Al������������У�Mg������������ƫ�������У�Al������)
(2)���ݵ��������������������Է�λ�жϡ�
�����·�����������������븺�������������ɸ�������������
(3)����ԭ�����������Һ�������ӵĶ���Ų����λ�жϡ�
��ԭ��صĵ������Һ�ڣ�����������������������������
(4)����ԭ��������淢����ת�����жϡ�
ԭ��صĸ�������������ԭ��Ӧ������������ԭ��Ӧ��
(5)X���������ӻ⡣
�����к�X��Ʒ������������X���л�ѧ�����ܽ⣬X�����������෴��X��Ʒ�ʽ��ͣ�����X�����������ڽ⣬X���为����
(6)X����������ɡ�
�����к�X���ϴ�������ɣ�һ�����������ܽ�H2�ĵ缫��Ӧ������X����������
(7)����X���ܱ�pH��ת�����жϡ�
����������ĵ缫��Ӧ��������ʹ�ý����缫�ܱߵ������Һ��pH������˹����к�X���ܱ�pH�����ˣ�����X����������
�������
- ��ѧʽ��ƽ�������ܽ���ϸ����
- ���ѵ����������жϻ�ѧƽ��״̬
- ���л�ѧ�����ӷ�Ӧ����ʽ�ܽ�
- ʲô��������Ӧ����һ��ѧ��Ӧԭ��
- ͬϵ����жϱ���һ��ѧ�л���ѧ
- ����ȼ������,����ȼ�շ���ʽ
- ����������ȼ�յĻ�ѧ����ʽ����������ϼ�
- ���л�ѧ����ʽ��ƽ�����ţ���һ��ѧ����
- ������ƽ��ѧ����ʽ����һ��ѧ
- �������ȡ��ô���룬��һ��ѧʵ��
- �����ᴿʵ����岽�輰�����������취
- �л������-��һ��ѧʵ��
- �����Ƽ�Ĺ��̣���ѧ��Ӧԭ��
- ��ϩ�ļӳɷ�Ӧ��һ��ѧ��Ӧԭ��
- ������ֲ���͵�����
- ���ϼ۱���һ��ѧ����������
- �жϻ�ѧƽ��ı�־��ѧ֪ʶ�ܽ�
- ʯ���͵ijɷ� ʯ���͵Ĺ��ܼ���;
- �����ͬ���칹�� ��һ��ѧ����
ѧϰ����
 ���л�ѧԭ��ع���ԭ��
���л�ѧԭ��ع���ԭ��