乙醇的性质
目的:认识乙醇的物理性质和化学性质。
用品:滴管、试管、试管夹、酒精灯、圆底烧瓶、玻璃导管、单孔橡皮塞、铁架台(带铁夹、直角夹、铁圈)、石棉网、烧杯、移液管、玻棒。无水酒精、普通酒精、钠、铁丝、浓硫酸、溴化钾、冰、无水硫酸铜。
原理:乙醇分子是由乙基C2H5—和羟基-OH组成的,羟基比较活泼,它决定着乙醇的主要性质,可跟氢卤酸反应,跟浓硫酸发生脱水反应。但是,乙醇的羟基里的氢原子也会被活泼金属所取代。准备和操作:
1.普通酒精里的水分 在两个干燥的试管里各加入少量无水硫酸铜粉末,再用滴管分别滴入无水酒精和普通酒精,前一个试管里的无水硫酸铜仍是白色,后一个试管里则呈蓝色。普通酒精里含水约4%(体积)。
2.乙醇在水里的溶解性 在一个试管里盛无水酒精2毫升,用滴管一滴滴地加入水2毫升,边加边振荡试管,可以观察到乙醇和水可以任何比例混溶。
3.乙醇和钠的反应 把2毫升无水酒精注入一干燥试管中,投入一小块钠,把试管浸在盛有冷水的烧杯里,以防止液体沸腾(反应放热)。当反应已不是很剧烈的时候,另取一个小试管用排气法收集所放出的气体,在试管口点燃,可以听到爆鸣声,证明放出的是氢气。以后试管里的反应逐渐减慢,这是因为钠的表面已覆盖上一层固态乙醇钠的缘故,可在酒精灯火焰上微微加热,使反应加快。
4.乙醇跟氢溴酸的反应 在一个圆底烧瓶里注入酒精3毫升,慢慢地加入密度为1.84克/厘米3的浓硫酸3毫升,振荡使它混和均匀。待混和液冷却以后,加水2毫升(避免溴化氢气体逸出),混和,再冷却。实验时,把圆底烧瓶装在铁架台上,加入溴化钾3克,立即塞上配有玻璃管的单孔橡皮塞。导管的末端伸入另一个盛水1毫升和有一些小冰块的试管里,这个试管再浸在盛有冰水的烧杯里。用酒精灯慢慢地加热烧瓶,使里面的液体平稳地沸腾。约 10分钟后,溴化钾已全部消失,这时试管里冰水下面就有溴乙烷沉积。停止加热后,把试管里的水倾去,用蒸馏水把溴乙烷洗涤一次,再用移液管把它吸出,注入另一个干净试管里。制得的溴乙烷大约有1毫升,用玻棒蘸一滴溴乙烷放在酒精灯火焰上燃烧,火焰的边缘会显现出特殊的绿色,这是溴乙烷燃烧的特征。
5.乙醇的氧化反应 乙醇在空气里能够燃烧,发生淡蓝色的火焰,生成二氧化碳和水,酒精灯的燃烧属于这种情况。在试管里加5毫升乙醇,把一端弯成螺旋状的铜丝放在酒精灯火焰上加热,使铜丝表面有一薄层黑色的氧化铜生成,立即把它插入盛有乙醇的试管里,如此反复操作数次,即能闻到有刺激性气味的乙醛生成。
6.乙醇的脱水反应 在加热时浓硫酸能使乙醇脱水,脱水有两种方式:分子内脱水、分子与分子间脱水。前者是属于消去反应,这在乙烯的制取和性质部分已讲述,后者请看后面的乙醚的生成部分。
用品:滴管、试管、试管夹、酒精灯、圆底烧瓶、玻璃导管、单孔橡皮塞、铁架台(带铁夹、直角夹、铁圈)、石棉网、烧杯、移液管、玻棒。无水酒精、普通酒精、钠、铁丝、浓硫酸、溴化钾、冰、无水硫酸铜。
原理:乙醇分子是由乙基C2H5—和羟基-OH组成的,羟基比较活泼,它决定着乙醇的主要性质,可跟氢卤酸反应,跟浓硫酸发生脱水反应。但是,乙醇的羟基里的氢原子也会被活泼金属所取代。准备和操作:
1.普通酒精里的水分 在两个干燥的试管里各加入少量无水硫酸铜粉末,再用滴管分别滴入无水酒精和普通酒精,前一个试管里的无水硫酸铜仍是白色,后一个试管里则呈蓝色。普通酒精里含水约4%(体积)。
2.乙醇在水里的溶解性 在一个试管里盛无水酒精2毫升,用滴管一滴滴地加入水2毫升,边加边振荡试管,可以观察到乙醇和水可以任何比例混溶。
3.乙醇和钠的反应 把2毫升无水酒精注入一干燥试管中,投入一小块钠,把试管浸在盛有冷水的烧杯里,以防止液体沸腾(反应放热)。当反应已不是很剧烈的时候,另取一个小试管用排气法收集所放出的气体,在试管口点燃,可以听到爆鸣声,证明放出的是氢气。以后试管里的反应逐渐减慢,这是因为钠的表面已覆盖上一层固态乙醇钠的缘故,可在酒精灯火焰上微微加热,使反应加快。
4.乙醇跟氢溴酸的反应 在一个圆底烧瓶里注入酒精3毫升,慢慢地加入密度为1.84克/厘米3的浓硫酸3毫升,振荡使它混和均匀。待混和液冷却以后,加水2毫升(避免溴化氢气体逸出),混和,再冷却。实验时,把圆底烧瓶装在铁架台上,加入溴化钾3克,立即塞上配有玻璃管的单孔橡皮塞。导管的末端伸入另一个盛水1毫升和有一些小冰块的试管里,这个试管再浸在盛有冰水的烧杯里。用酒精灯慢慢地加热烧瓶,使里面的液体平稳地沸腾。约 10分钟后,溴化钾已全部消失,这时试管里冰水下面就有溴乙烷沉积。停止加热后,把试管里的水倾去,用蒸馏水把溴乙烷洗涤一次,再用移液管把它吸出,注入另一个干净试管里。制得的溴乙烷大约有1毫升,用玻棒蘸一滴溴乙烷放在酒精灯火焰上燃烧,火焰的边缘会显现出特殊的绿色,这是溴乙烷燃烧的特征。
5.乙醇的氧化反应 乙醇在空气里能够燃烧,发生淡蓝色的火焰,生成二氧化碳和水,酒精灯的燃烧属于这种情况。在试管里加5毫升乙醇,把一端弯成螺旋状的铜丝放在酒精灯火焰上加热,使铜丝表面有一薄层黑色的氧化铜生成,立即把它插入盛有乙醇的试管里,如此反复操作数次,即能闻到有刺激性气味的乙醛生成。
6.乙醇的脱水反应 在加热时浓硫酸能使乙醇脱水,脱水有两种方式:分子内脱水、分子与分子间脱水。前者是属于消去反应,这在乙烯的制取和性质部分已讲述,后者请看后面的乙醚的生成部分。
推荐内容
教育新鲜事
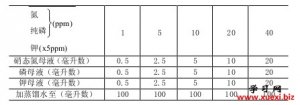 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有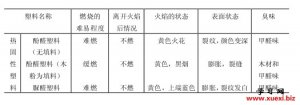 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的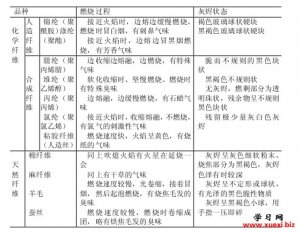 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维