乙醇分子结构的确定
目的:通过一定量乙醇和钠反应所产生的氢气体积的测定,确定乙醇的分子结构。
用品:圆底烧瓶、双孔橡皮塞、分液漏斗、铁架台(带铁夹)、弹簧夹、导管、橡皮管、广口瓶、量筒、酒精灯。钠、无水酒精。
原理:乙醇分子可能有下列两种结构:
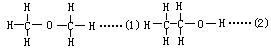
实验时,从分液漏斗把无水酒精一滴滴地全部加入烧瓶里。加入酒精的速度要慢,让酒精跟钠能很好地接触。这时反应生成的氢气就把广口瓶的水压入量筒中,压出的水的体积,就等于放出氢气的体积。当烧瓶里的反应终止后,用酒精灯在烧瓶外微微加热,观察量筒中水位是否上升。如果水位不再上升,表示反应已经完毕,让装置冷却。调整大量筒的位置,使广口瓶和量筒中水处于同一平面,夹紧导管上的夹子,记下量筒水面的刻度。从量筒中水的体积,加上广口瓶导出管水柱的体积,再减去加入烧瓶里酒精的体积,就得到酒精跟钠反应生成氢气的体积。根据计算,1摩尔乙醇反应所得氢气体积是11.2升,则一个乙醇分子中含有一个可被置换的氢原子,并可推知此氢原子与氧原子相结合,故其结构式为C2H5OH。
注意事项:
1.整个装置要不漏气。无水酒精必须是化学纯的,所用的钠应稍过量些,金属钠的外皮必须切尽,把钠切成薄片,浸在二甲苯里,微热使熔,用玻棒将熔钠搅成碎粒。愈细,接触酒精的面积愈大,反应就进行得愈充分。反应结束后,拆卸装置时,应加入过量乙醇使剩余的钠反应掉,切不可用水冲洗。
2.广口瓶和量筒的容积要与乙醇的用量相适应。根据本实验的乙醇用量,它们的容积必须大于600毫升,在装置上,排水管必须插入能排出 600毫升体积的水面下,否则氢气会从液面逸出。
3.无水酒精要一滴一滴地加入,并轻轻地振荡烧瓶,使乙醇和钠充分接触。其它实验方法:
准备:
1.将已刮除氧化膜外皮的金属钠约0.5克,放入小试管里,加入甲苯或精制煤油约15毫升,剪成很短的玻璃纤维(最好用高铝纤维)1角匙。
2.将试管加热,到钠熔化后继续加热10~15秒钟,然后离开火焰,加塞。
3.用干抹布包住塞子及试管口,大拇指紧压塞子,将试管上下猛烈振荡约半分钟,使钠分散成钠粉,然后将煤油及钠粉移入大试管,加塞备用。
操作:1.用滴管从小量筒中吸取0.6毫升无水乙醇,以快速度注入大试管,随即将塞子紧塞,并立即用排水集气法收集H2于量筒中。2.乙醇跟钠粉立即进行反应。当反应速度减慢时,用微火进行加热,到H2不再放出时,撤火,并立即把塞子打开。
用品:圆底烧瓶、双孔橡皮塞、分液漏斗、铁架台(带铁夹)、弹簧夹、导管、橡皮管、广口瓶、量筒、酒精灯。钠、无水酒精。
原理:乙醇分子可能有下列两种结构:
实验时,从分液漏斗把无水酒精一滴滴地全部加入烧瓶里。加入酒精的速度要慢,让酒精跟钠能很好地接触。这时反应生成的氢气就把广口瓶的水压入量筒中,压出的水的体积,就等于放出氢气的体积。当烧瓶里的反应终止后,用酒精灯在烧瓶外微微加热,观察量筒中水位是否上升。如果水位不再上升,表示反应已经完毕,让装置冷却。调整大量筒的位置,使广口瓶和量筒中水处于同一平面,夹紧导管上的夹子,记下量筒水面的刻度。从量筒中水的体积,加上广口瓶导出管水柱的体积,再减去加入烧瓶里酒精的体积,就得到酒精跟钠反应生成氢气的体积。根据计算,1摩尔乙醇反应所得氢气体积是11.2升,则一个乙醇分子中含有一个可被置换的氢原子,并可推知此氢原子与氧原子相结合,故其结构式为C2H5OH。
注意事项:
1.整个装置要不漏气。无水酒精必须是化学纯的,所用的钠应稍过量些,金属钠的外皮必须切尽,把钠切成薄片,浸在二甲苯里,微热使熔,用玻棒将熔钠搅成碎粒。愈细,接触酒精的面积愈大,反应就进行得愈充分。反应结束后,拆卸装置时,应加入过量乙醇使剩余的钠反应掉,切不可用水冲洗。
2.广口瓶和量筒的容积要与乙醇的用量相适应。根据本实验的乙醇用量,它们的容积必须大于600毫升,在装置上,排水管必须插入能排出 600毫升体积的水面下,否则氢气会从液面逸出。
3.无水酒精要一滴一滴地加入,并轻轻地振荡烧瓶,使乙醇和钠充分接触。其它实验方法:
准备:
1.将已刮除氧化膜外皮的金属钠约0.5克,放入小试管里,加入甲苯或精制煤油约15毫升,剪成很短的玻璃纤维(最好用高铝纤维)1角匙。
2.将试管加热,到钠熔化后继续加热10~15秒钟,然后离开火焰,加塞。
3.用干抹布包住塞子及试管口,大拇指紧压塞子,将试管上下猛烈振荡约半分钟,使钠分散成钠粉,然后将煤油及钠粉移入大试管,加塞备用。
操作:1.用滴管从小量筒中吸取0.6毫升无水乙醇,以快速度注入大试管,随即将塞子紧塞,并立即用排水集气法收集H2于量筒中。2.乙醇跟钠粉立即进行反应。当反应速度减慢时,用微火进行加热,到H2不再放出时,撤火,并立即把塞子打开。
推荐内容
教育新鲜事
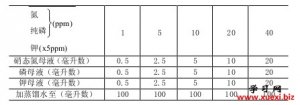 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有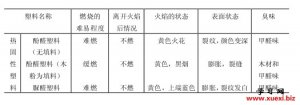 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的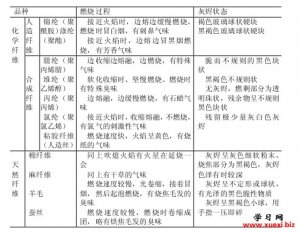 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维