氢氧化镁的生成和性质
目的:认识氢氧化镁的制取方法和性质。
用品:试管。氯化镁溶液(0.2摩/升)、氢氧化钠溶液(2摩/升)、盐酸、氯化铵饱和溶液。
原理:实验室里用强碱跟镁盐溶液反应来制取氢氧化镁。MgCl2+2NaOH=Mg(OH)2↓+2NaCl 氢氧化镁是中强碱,能跟酸反应生成盐和水。氢氧化镁难溶于水,但易溶于氯化铵溶液中,因为氯化铵溶液具有酸性(水解)。Mg(OH)2+2NH4+=Mg2++2NH3·H2O操作:
1.氢氧化镁的生成在试管里加入5毫升0.2摩/升氯化镁溶液,再滴加2摩/升氢氧化钠溶液,直至不再析出白色沉淀为止。
2.氢氧化镁跟酸的反应将上述试管里的上层清液倾去,白色的氢氧化镁沉淀用蒸馏水洗涤后取出一半,加入另一支试管待用。再向试管里滴加2摩/升盐酸溶液,振荡,沉淀溶解。
3.氢氧化镁跟铵盐溶液的反应向另一支加入氢氧化镁沉淀的试管里滴加氯化铵饱和溶液,振荡,沉淀溶解。
用品:试管。氯化镁溶液(0.2摩/升)、氢氧化钠溶液(2摩/升)、盐酸、氯化铵饱和溶液。
原理:实验室里用强碱跟镁盐溶液反应来制取氢氧化镁。MgCl2+2NaOH=Mg(OH)2↓+2NaCl 氢氧化镁是中强碱,能跟酸反应生成盐和水。氢氧化镁难溶于水,但易溶于氯化铵溶液中,因为氯化铵溶液具有酸性(水解)。Mg(OH)2+2NH4+=Mg2++2NH3·H2O操作:
1.氢氧化镁的生成在试管里加入5毫升0.2摩/升氯化镁溶液,再滴加2摩/升氢氧化钠溶液,直至不再析出白色沉淀为止。
2.氢氧化镁跟酸的反应将上述试管里的上层清液倾去,白色的氢氧化镁沉淀用蒸馏水洗涤后取出一半,加入另一支试管待用。再向试管里滴加2摩/升盐酸溶液,振荡,沉淀溶解。
3.氢氧化镁跟铵盐溶液的反应向另一支加入氢氧化镁沉淀的试管里滴加氯化铵饱和溶液,振荡,沉淀溶解。
推荐内容
教育新鲜事
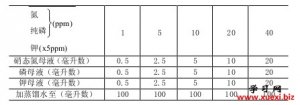 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有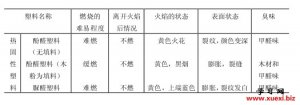 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的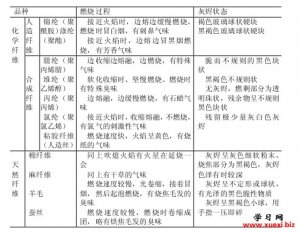 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维