苏尔维制碱法的实验
用品:烧杯、试管、广口瓶、分液漏斗、温度计、铁架台、铁夹、螺旋夹、酒精灯。氯化钠(化学纯、精盐也可用)、大理石、盐酸、浓氨水。
原理:利用二氧化碳和氨气在饱和的食盐溶液中进行反应,首先是二氧化碳和氨在溶液中反应生成碳酸氢铵,碳酸氢铵再和氯化钠反应生成溶解度轻小的碳酸氢钠和氯化铵。把碳酸氢钠分离出来后进行煅烧,即得碳酸钠的成品。而氯化铵又可和氢氧化钙反应可以得到氨气(可用作原料),氢氧化钙可由生石灰消化而来,生石灰又可由石灰石煅烧制得,同时有二氧化碳产生,二氧化碳又可作原料。因此,最终的原料仅是石灰石和食盐。
操作:1.在广口瓶A中装入大理石100克及少量的水,分液漏斗中加入大半漏斗的盐酸,用双孔橡皮塞插入瓶中(带有直角玻璃导管)。也可使用启普发生器作为实验装置。2.广口瓶B作洗气用,瓶内放入约1/3瓶的水,橡皮塞上配有两根直角玻璃导管,塞紧瓶口,导管插入水内,以洗掉盐酸酸雾和氯化氢气体。3.称取3克化学纯的氯化钠,放入5毫升的水,再加5毫升的浓氨水(比重为0.91),使其溶解。待完全溶解后,倒入 C管,再将C管浸入盛有水的烧杯内。如室温在15℃以下,可以加热盛水的烧杯,使温度保持在35~140℃,以加快反应速度。4.用橡皮管把A、B、C三个瓶、管连接好,检查气密性后,打开分液漏斗的活塞,使盐酸慢慢地流入 A瓶中。导管中的螺旋夹可以调节二氧化碳的气流速度,当有二氧化碳通入C管时,可经常小心摇动。约 20分钟左右,可观察到在C管中有混浊现象,再继续通入二氧化碳,不久即有碳酸氢钠沉淀生成。5.把过滤得到的碳酸氢钠,放入试管中小心加热(试管口向下倾斜),使其分解即得碳酸钠。
注意事项:1.氨水的浓度,在达到9~10.5%(比重0.96左右)都较为适宜。2.二氧化碳和氨的反应是放热反应,但如果室温在15℃以下,反应速度很慢,实践证明在 40℃左右能较快地生成 NaHCO3。如室温在 25℃以上,则可不必加热。3.二氧化碳的速度不要过猛,只要使气泡一个接一个地均匀产生即可。
原理:利用二氧化碳和氨气在饱和的食盐溶液中进行反应,首先是二氧化碳和氨在溶液中反应生成碳酸氢铵,碳酸氢铵再和氯化钠反应生成溶解度轻小的碳酸氢钠和氯化铵。把碳酸氢钠分离出来后进行煅烧,即得碳酸钠的成品。而氯化铵又可和氢氧化钙反应可以得到氨气(可用作原料),氢氧化钙可由生石灰消化而来,生石灰又可由石灰石煅烧制得,同时有二氧化碳产生,二氧化碳又可作原料。因此,最终的原料仅是石灰石和食盐。
操作:1.在广口瓶A中装入大理石100克及少量的水,分液漏斗中加入大半漏斗的盐酸,用双孔橡皮塞插入瓶中(带有直角玻璃导管)。也可使用启普发生器作为实验装置。2.广口瓶B作洗气用,瓶内放入约1/3瓶的水,橡皮塞上配有两根直角玻璃导管,塞紧瓶口,导管插入水内,以洗掉盐酸酸雾和氯化氢气体。3.称取3克化学纯的氯化钠,放入5毫升的水,再加5毫升的浓氨水(比重为0.91),使其溶解。待完全溶解后,倒入 C管,再将C管浸入盛有水的烧杯内。如室温在15℃以下,可以加热盛水的烧杯,使温度保持在35~140℃,以加快反应速度。4.用橡皮管把A、B、C三个瓶、管连接好,检查气密性后,打开分液漏斗的活塞,使盐酸慢慢地流入 A瓶中。导管中的螺旋夹可以调节二氧化碳的气流速度,当有二氧化碳通入C管时,可经常小心摇动。约 20分钟左右,可观察到在C管中有混浊现象,再继续通入二氧化碳,不久即有碳酸氢钠沉淀生成。5.把过滤得到的碳酸氢钠,放入试管中小心加热(试管口向下倾斜),使其分解即得碳酸钠。
注意事项:1.氨水的浓度,在达到9~10.5%(比重0.96左右)都较为适宜。2.二氧化碳和氨的反应是放热反应,但如果室温在15℃以下,反应速度很慢,实践证明在 40℃左右能较快地生成 NaHCO3。如室温在 25℃以上,则可不必加热。3.二氧化碳的速度不要过猛,只要使气泡一个接一个地均匀产生即可。
推荐内容
教育新鲜事
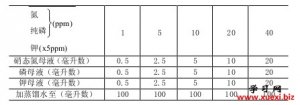 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有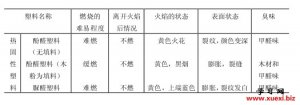 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的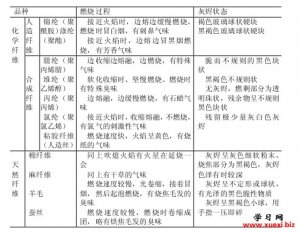 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维