浓度对化学反应速度的影响
用品:玻璃点滴板。0.1摩/升H2SO4溶液、0.1摩/升Na2S2O3溶液、蒸馏水。
操作(水平投影):将玻璃点滴板放在投影仪的载物台上。向玻璃点滴板的三个孔中分别滴入0.1摩/升的Na2S2O3溶液3滴、2滴和1滴。然后在滴2滴的Na2S2O3溶液的孔中滴入1滴蒸馏水;在滴1滴的Na2S2O3溶液的孔中滴入2滴蒸馏水。再向三个孔中分别滴入0.1摩/升H2SO4溶液各1滴。Na2S2O3溶液与酸作用,有硫黄析出,因此,在三个不同浓度的 Na2S2O3溶液中滴入硫酸后,发现浓度大的Na2S2O3溶液先浑浊(有硫黄析出),浓度小的Na2S2O3溶液后浑浊。这说明浓度大,反应速度快。反应式如下:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O
操作(水平投影):将玻璃点滴板放在投影仪的载物台上。向玻璃点滴板的三个孔中分别滴入0.1摩/升的Na2S2O3溶液3滴、2滴和1滴。然后在滴2滴的Na2S2O3溶液的孔中滴入1滴蒸馏水;在滴1滴的Na2S2O3溶液的孔中滴入2滴蒸馏水。再向三个孔中分别滴入0.1摩/升H2SO4溶液各1滴。Na2S2O3溶液与酸作用,有硫黄析出,因此,在三个不同浓度的 Na2S2O3溶液中滴入硫酸后,发现浓度大的Na2S2O3溶液先浑浊(有硫黄析出),浓度小的Na2S2O3溶液后浑浊。这说明浓度大,反应速度快。反应式如下:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O
推荐内容
教育新鲜事
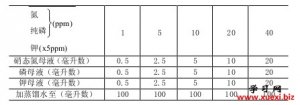 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有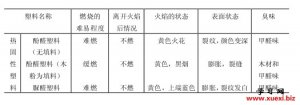 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的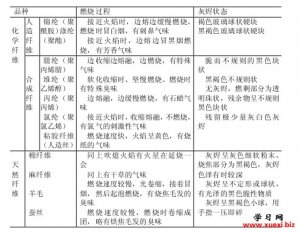 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维