接触法制三氧化硫
目的:制取三氧化硫,了解三氧化硫的性质,认识硫酸的生产过程。
用品:铁夹、气唧、反应管、安瓿、蒸发皿。硫粉、浓硫酸、蒸馏水、氯化钡溶液、盐酸、紫色石蕊试液、重铬酸铵、粗食盐。
准备:将2 克硫粉,放在蒸发皿中加热,待熔化时,加入2克石棉绒,用玻棒搅拌,使石棉绒均匀沾上熔硫,成为硫棉。趁热撕成蚕豆大小块,冷却后备用。用1克重铬酸铵晶体,放在试管中,使其受热分解成Cr2O3。继续加热至干燥,装入反应管细管部分。Cr2O3两边,用细铜丝阻塞。
操作:酒精灯加热催化剂3分钟后,用镊子夹持硫棉一块,点燃。置于反应管粗管中,塞上连有气唧的橡皮塞。微微掀动气唧,鼓入空气,使硫继续燃烧生成二氧化硫。当 SO2与空气的混和物通过催化剂时,能见到催化剂红热,同时在反应管右部导管口有白烟冒出。当 SO3通过水吸收器时,产生大量酸雾而冒“烟”,通过浓硫酸吸收器时无此现象。取下水、浓硫酸吸收器,将SO3通入安瓿,并将安瓿没入冰盐水中冷却。片刻即可观察到白色 SO3晶体生成。反应管与吸收器连接处的乳胶管,由于炭化而变黑。在上述通SO3的蒸馏水中,加入BaCl2 溶液,立即出现浑浊。用盐酸酸化,浑浊不消失。
注意事项:1.鼓气不要太急太快,要使硫棉充分燃烧。2.欲制SO3晶体,导管和安瓿要极为干燥(要预先烘过,用橡皮塞封口,用时打开)。3.装置中乳胶接头要短,以免腐蚀炭化。
用品:铁夹、气唧、反应管、安瓿、蒸发皿。硫粉、浓硫酸、蒸馏水、氯化钡溶液、盐酸、紫色石蕊试液、重铬酸铵、粗食盐。
准备:将2 克硫粉,放在蒸发皿中加热,待熔化时,加入2克石棉绒,用玻棒搅拌,使石棉绒均匀沾上熔硫,成为硫棉。趁热撕成蚕豆大小块,冷却后备用。用1克重铬酸铵晶体,放在试管中,使其受热分解成Cr2O3。继续加热至干燥,装入反应管细管部分。Cr2O3两边,用细铜丝阻塞。
操作:酒精灯加热催化剂3分钟后,用镊子夹持硫棉一块,点燃。置于反应管粗管中,塞上连有气唧的橡皮塞。微微掀动气唧,鼓入空气,使硫继续燃烧生成二氧化硫。当 SO2与空气的混和物通过催化剂时,能见到催化剂红热,同时在反应管右部导管口有白烟冒出。当 SO3通过水吸收器时,产生大量酸雾而冒“烟”,通过浓硫酸吸收器时无此现象。取下水、浓硫酸吸收器,将SO3通入安瓿,并将安瓿没入冰盐水中冷却。片刻即可观察到白色 SO3晶体生成。反应管与吸收器连接处的乳胶管,由于炭化而变黑。在上述通SO3的蒸馏水中,加入BaCl2 溶液,立即出现浑浊。用盐酸酸化,浑浊不消失。
注意事项:1.鼓气不要太急太快,要使硫棉充分燃烧。2.欲制SO3晶体,导管和安瓿要极为干燥(要预先烘过,用橡皮塞封口,用时打开)。3.装置中乳胶接头要短,以免腐蚀炭化。
相关文章
推荐内容
教育新鲜事
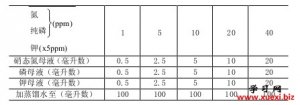 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有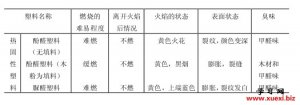 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的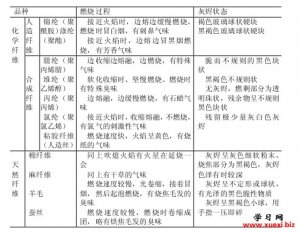 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维