过氧化钠吸收二氧化碳放出氧气
目的:掌握Na2O2与CO2的反应及其气体体积之间的定量关系。
用品:250毫升医用盐水瓶、安瓿、水槽、尖嘴长玻管。过氧化钠、浓硫酸、稀硫酸、碳酸钠、酚酞试液。准备:取盐水瓶一个,装满水后,将水倒入量筒,测出其容积,并在容积一半处做上标记。干燥盐水瓶,配上带有拉成尖嘴、长 20~25厘米玻璃导管的橡皮塞。导管尖嘴正好伸入瓶容积一半处。导管另一端套上一小段橡皮管,并夹上弹簧夹。计算在实验条件(指温度、压强需换算成标准状态)下,该容积的 CO2与Na2O2的反应量。在分析天平上称取所需的Na2O2(用安瓿代替称量瓶)。
操作:用Na2CO3与稀H2SO4反应,制取CO2气体,经浓硫酸洗气后,用向上排空气法收集于已测知容积的干燥盐水瓶中,收满即可。连同安瓿,将Na2O2放入充满CO2的盐水瓶中,塞上带尖嘴导管的橡皮塞,振摇,使完全反应。将玻璃导管没入水槽(水中滴有酚酞)中,打开弹簧夹。由于Na2O2与CO2反应,使盐水瓶内产生负压,形成喷泉。进入瓶内的水变成红色。喷泉停止,水正好充满盐水瓶容积的一半(在刻度处)。用带有余烬的木条伸入瓶内,木条复燃,证明瓶内的气体是氧气。
注意事项:Na2O2过量,将使氧气的量超过盐水瓶容积的一半,引起较大误差。
用品:250毫升医用盐水瓶、安瓿、水槽、尖嘴长玻管。过氧化钠、浓硫酸、稀硫酸、碳酸钠、酚酞试液。准备:取盐水瓶一个,装满水后,将水倒入量筒,测出其容积,并在容积一半处做上标记。干燥盐水瓶,配上带有拉成尖嘴、长 20~25厘米玻璃导管的橡皮塞。导管尖嘴正好伸入瓶容积一半处。导管另一端套上一小段橡皮管,并夹上弹簧夹。计算在实验条件(指温度、压强需换算成标准状态)下,该容积的 CO2与Na2O2的反应量。在分析天平上称取所需的Na2O2(用安瓿代替称量瓶)。
操作:用Na2CO3与稀H2SO4反应,制取CO2气体,经浓硫酸洗气后,用向上排空气法收集于已测知容积的干燥盐水瓶中,收满即可。连同安瓿,将Na2O2放入充满CO2的盐水瓶中,塞上带尖嘴导管的橡皮塞,振摇,使完全反应。将玻璃导管没入水槽(水中滴有酚酞)中,打开弹簧夹。由于Na2O2与CO2反应,使盐水瓶内产生负压,形成喷泉。进入瓶内的水变成红色。喷泉停止,水正好充满盐水瓶容积的一半(在刻度处)。用带有余烬的木条伸入瓶内,木条复燃,证明瓶内的气体是氧气。
注意事项:Na2O2过量,将使氧气的量超过盐水瓶容积的一半,引起较大误差。
推荐内容
教育新鲜事
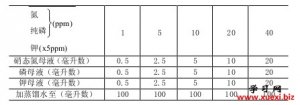 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有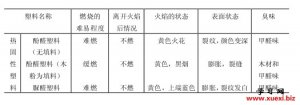 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的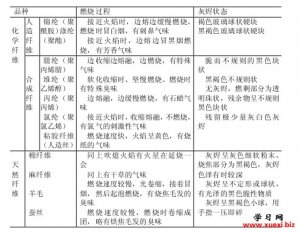 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维