铜的晶体
“铜晶体”这一名词听起来非常陌生,这种实物也很少有人见过,但它的确是存在的。不信,你可以按照以下的方法做一个有趣的实验。
先配制两种铜盐的溶液:一种是浓的,25毫升2M 硝酸铜溶液;另一种是稀的,25毫升0.2M硝酸铜溶液。在后一种溶液中还要加入2—3滴浓硝酸。



取一支试管(容积为70—80毫升),配上一个橡皮塞或软木塞,塞子的中央钻一细孔,孔内插入一根粗铜丝(可用刮掉漆膜的漆包线代替)。铜丝要稍粗一点,太细了在溶液中立不起来。把试管放在试管架上,先倒入25毫升2M硝酸铜溶液,然后沿着试管壁慢慢地再倒入25毫升0.2M硝酸铜溶液。注意,切勿使这两种浓度不同的溶液混合起来。 浓的硝酸铜溶液比较重,就在试管的下半部;稀的硝酸铜溶液比较轻,在试管的上半部,我们应该能够清楚地看到它们之间有明显的分界面。最后,小心地把带有塞子的粗铜丝插到试管中。插时,动作要既轻又慢,不要把两种浓度不同的溶液搞混了。
过了几天以后,你会看到铜丝的下端附着了光亮的铜晶体。如果晶体不太多,还看不清楚,你也不必焦急,再等上几天,一定会长出美丽的铜晶体。把铜丝从溶液中取出,用水洗净后,再用放大镜观察,晶体的形状就更为清晰可见了。你还可以把它保存起来,供别人欣赏。
“铜晶体”这一名词听起来非常陌生,这种实物也很少有人见过,但它的确是存在的。不信,你可以按照以下的方法做一个有趣的实验。 先配制两种铜盐的溶液:一种是浓的,25毫升2M 硝酸铜溶液;另一种是稀的,25毫升0.2M硝酸铜溶液。在后一种溶液中还要加入2—3滴浓硝酸。锌离子:Zn—→Zn2++2e然后,电子流入正极(铜片),溶液中的氢离子获得电子,因此在正极上产生氢气:2H++2e—→H2↑
“铜晶体”这一名词听起来非常陌生,这种实物也很少有人见过,但它的确是存在的。不信,你可以按照以下的方法做一个有趣的实验。
先配制两种铜盐的溶液:一种是浓的,25毫升2M 硝酸铜溶液;另一种是稀的,25毫升0.2M硝酸铜溶液。在后一种溶液中还要加入2—3滴浓硝酸。
推荐内容
教育新鲜事
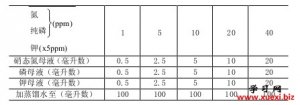 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有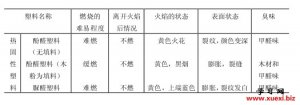 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的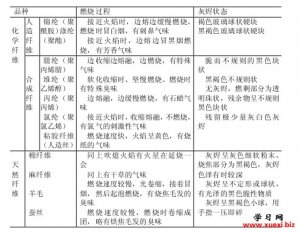 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维