初中化学方程式配平技巧讲解
化学姐
在化学反应的过程中,遵守质量守恒定律。为了使方程式满足质量守恒定律,需要对方程式加以配平。
1、最小公倍数法,适用于一些较为简单的化学方程式的配平。
2、以磷燃烧为例,先写出反应的符号表达式。
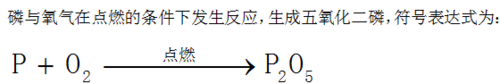
3、在这个反应中,氧元素的数据较大,所以我们选择氧元素计算最大公倍数。左右两边氧的系数的最小公倍数为2×5=10,所以应有10个氧原子参与反应。在将10除以每个化学式中氧原子的数量,就可以得到对应的化学式的系数。
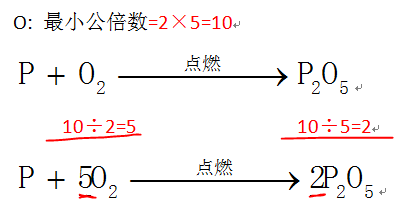
4、最后再根据质量守恒定律,得出其他系数。由已知的系数可得参与反应的磷原子的数量为4,所以P前的系数为4。最后将箭头改为等号,配平完成。

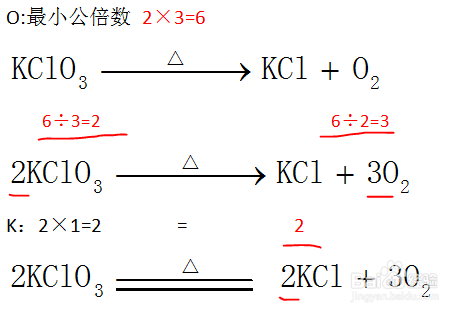
5、氯酸钾分解等方程式,也可采用这种方法配平。
1、观察法也适用于一些简单的方程式,用观察法配平的关键是搞清反应的实质。
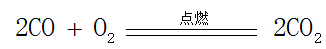
2、例如,一氧化碳燃烧就可以用这种方法配平。观察一氧化碳燃烧的符号表达式,可以发现一氧化碳燃烧实质是每个一氧化碳分子得到一个氧原子,变为二氧化碳。

3、因为氧分子中有2个氧原子,所以每2个CO从一个O2分子中各得到一个氧原子,变为2个CO2分子。因此反应方程式中CO,O2,CO2的系数分别为1,2,2。
4、过氧化氢分解也可以这种方法配平。其反应实质是每个过氧化氢分子失去1个氧原子,变成1个水分子。

5、酸、碱、盐之间的反应,也可以用这种方法配平。例如,氢氧化钠与硫酸中和,其本质是氢氧根离子与氢离子结合生成水分子。因为每个H2SO4中有2个氢离子参与反应,所以每两个NaOH与一个H2SO4反应,生成一个Na2SO4和2个水分子。
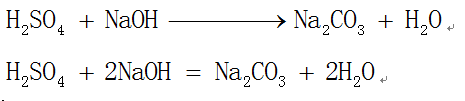
对于一些较为复杂的化学方程式,无法使用最小公倍数法,也很难采用观察法,这时可以考虑采用待定系数法。采用待定系数法,并不是每个化学式前都设一个未知数,未知数的数量越少越好。
例如,在加热高锰酸钾制取氧气的方程式中,可先设K2MnO4前的系数为a,则显然有2a个K参与反应,所以KMnO4前的系数应为2a。
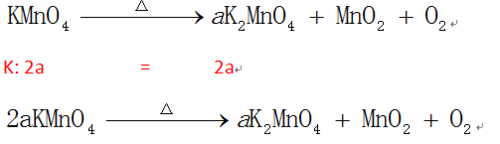
再根据质量守恒定律,得出其他化学式前的系数。
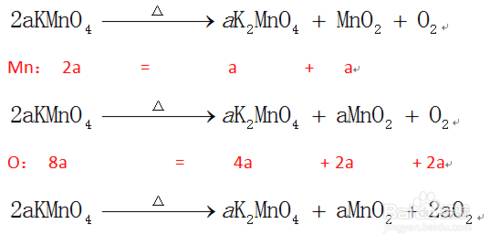
最后求出系数的最大公因数为a,各系数都除以最大公因数,得到KMnO4,K2MnO4,MnO2,O2的系数分别为2,1,1,1.
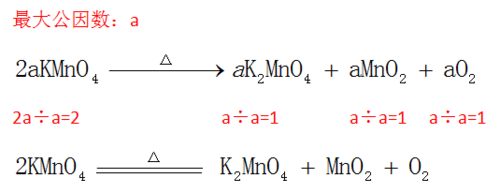
再看一个较为复杂的反应:
XeO3+MnSO4+H2O→HMnO4+Xe+H2SO4
可先设XeO3的系数为a,MnSO4的系数为b。
由Xe元素的质量守恒,可得Xe前的系数为a;
由Mn元素的质量守恒,可得HMnO4前的系数为b;
由S元素的质量守恒,可得H2SO4前的系数也为b。
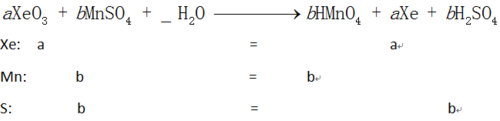
由H元素质量守恒可得H2O前的系数为1.5b;
O元素前的系数为4b-3a;
显然1.5b=4b-3a,变形可得6a=5b。
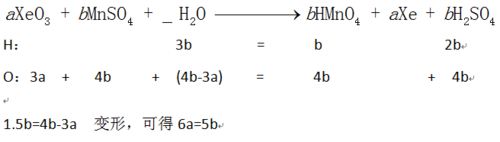
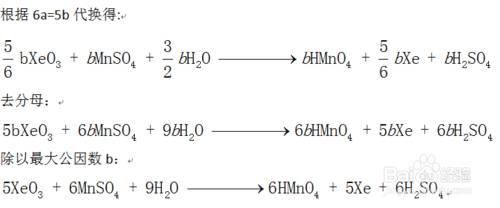
根据6a=5b,将所有的a替换为b,然后去分母。最后除以最大公因数,配平完成。

相关文章
- 为了学好化学,必须做一定的练习
- 学化学,离不开大量的练习
- 初中化学高效学习方法
- 记忆化学式,化学方程式应采用化学法
- 初中化学 | 重点化学方程式和实验动图合集,收藏!
- 初中必背的77个化学方程式。
- 2019年中考化学加油站:初中化学方程式现象总结(详细,经典!!
- 【每日一题】中考化学基础练习:化学方程式
- 化学必修一化学方程式大总结!
- 中考化学易错点汇总:化学方程式中常出错的气体符号与沉淀符号
- 化学方程式中“↑”和“↓”的用法
- 中考化学化学方程式考点梳理,收藏!
- 吐血推荐,化学方程式配平“神套路”,不用后悔!
- 学霸教你:6招快速解决“化学方程式配平”问题!
- 【知识要点】2019中考化学方程式考点梳理,收藏!
- 质量守恒和化学方程式知识点全归纳,还不会的同学赶快看!
- 【知识点】质量守恒和化学方程式知识点全归纳,赶快看!
- 最完整版初中化学方程式总结!拿去好好背!
- 初中化学重点化学方程式和实验动图合集,赶紧收藏!
- 初中化学方程式大汇总、狙击中考化学!
推荐内容
教育新鲜事
 为了学好化学,必须做一
为了学好化学,必须做一 初三化学入门就算顺利通
初三化学入门就算顺利通 提高初中化学成绩的五种
提高初中化学成绩的五种 初中生快速提高化学成绩
初中生快速提高化学成绩