电解水时为什么要加入少量电解质
从纯水的导电实验测得,在25℃时,纯水中H+离子和OH-离子的浓度等于10-7摩/升。因此,实际上观察不到水的电解现象。这是因为,当 H+离子在阴极上得到电子而生成氢气时,破坏了附近水的电离平衡,最终使阴极附近的 OH-离子的数目相对地增多,这就使阴极附近的溶液带负电,它会吸引其它的H+离子并阻止H+离子继续在阴极上放电。阳极的情况与此相仿。若在水中加入少量某种强电解质,由于这些强电解质在溶液中全部电离,离子数目增多,在电场的影响下分别向两极移动,这样,水在电解时,阴阳两极附近的溶液里离子的电荷得到平衡,使水的电解能继续进行。以纯水中加入Na2SO4通电分解为例,在水溶液中存在着Na+、H+、SO2-4、OH-四种离子。根据它们电极电位的高低,在阳极,OH-离子放电,产物是氧气。
随着OH-离子不断放电,如前所述,阳极附近聚集了相对多的H+离子时,由于SO2-4离子不断迁移到阳极附近,使阳极附近溶液里离子的电荷得到了平衡。在阴极,H+离子放电,产物是氢气。同理,阴极附近溶液里离子的电荷也得到平衡。这样,水的电离平衡就不断向右移动,H+离子和OH-离子不断地在两极上放电,但Na2SO4并不发生电解,它只是起着使电极附近电解溶液里的电荷迅速得到平衡,从而使水的电解能继续进行的作用。
随着OH-离子不断放电,如前所述,阳极附近聚集了相对多的H+离子时,由于SO2-4离子不断迁移到阳极附近,使阳极附近溶液里离子的电荷得到了平衡。在阴极,H+离子放电,产物是氢气。同理,阴极附近溶液里离子的电荷也得到平衡。这样,水的电离平衡就不断向右移动,H+离子和OH-离子不断地在两极上放电,但Na2SO4并不发生电解,它只是起着使电极附近电解溶液里的电荷迅速得到平衡,从而使水的电解能继续进行的作用。
相关文章
推荐内容
教育新鲜事
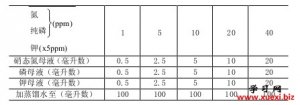 土壤有效养分的化学速测
土壤有效养分的化学速测 利用阿斯匹林进行几种有
利用阿斯匹林进行几种有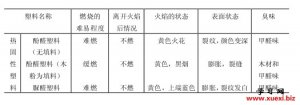 用燃烧法鉴别几种常用的
用燃烧法鉴别几种常用的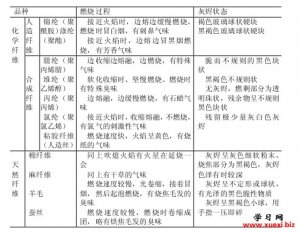 用燃烧法鉴别各种纤维
用燃烧法鉴别各种纤维