Fe(OH)2与Fe(OH)3胶体的制备

高中学习帮小程序(点击进入)

1.Fe(OH)2的制备
Fe(OH)2易被空气中的氧气氧化,生成Fe(OH)3,所以在制备Fe(OH)2时:
(1)要确保Fe2+溶液中无Fe3+,故需加Fe粉,把Fe3+转化为Fe2+。
(2)要尽量减少与O2的接触,故采取加热的方法赶走所需溶液中溶解的O2,冷却后再反应;同时应防止空气中的O2再溶于溶液,常用的方法有三种:
①反应在试管底部进行。
如图甲,这是中学阶段唯一把胶头滴管插入反应溶液的实验。
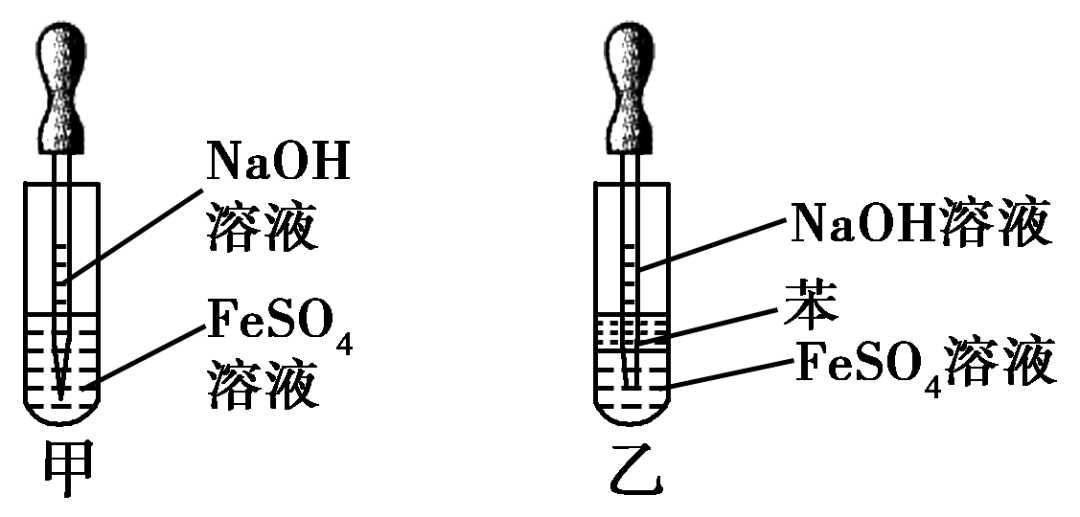
②加隔氧剂,如加入汽油、苯等比水轻的有机溶剂。
如图乙,由于苯的液封作用,防止了生成的Fe(OH)2被氧化,因而可较长时间观察到白色的Fe(OH)2沉淀。
③利用反应产生非氧化性气体(或通入非氧化性气体)赶走空气的方法。
如方案一、方案二,此方法可以长时间观察到白色的Fe(OH)2沉淀。
方案一:
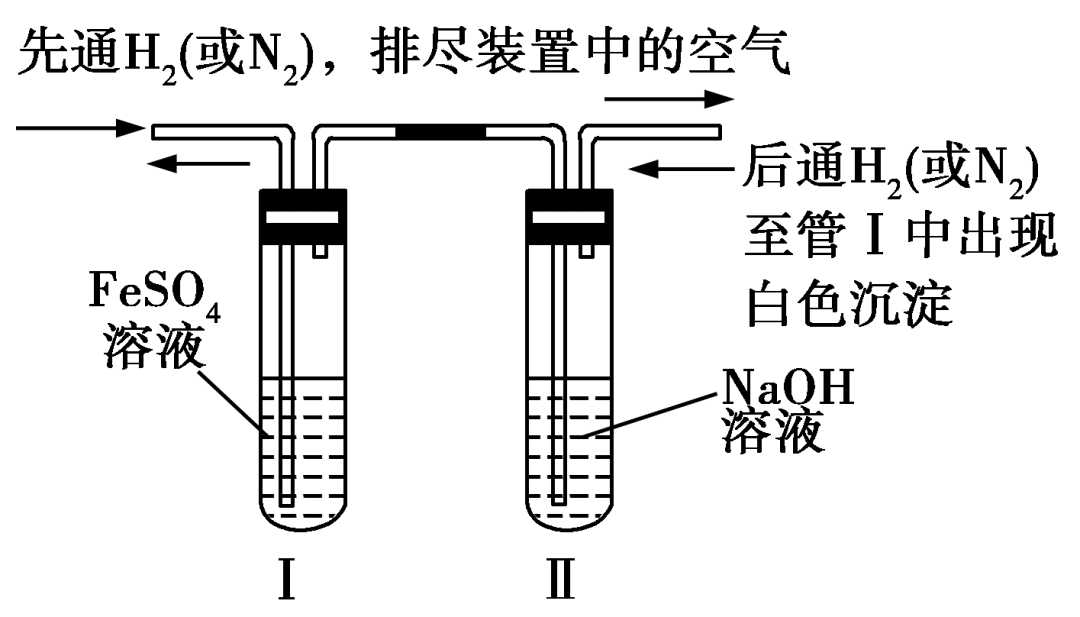
该方法是先用非氧化性气体排尽溶液和装置内的空气,再把试管Ⅱ中的NaOH溶液压入试管Ⅰ中反应。
方案二:
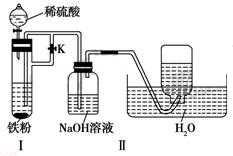
该方法是先在装置Ⅰ中产生FeSO4溶液,并利用产生的H2排尽两溶液和装置内的空气,再关闭止水夹K,利用产生的H2把FeSO4溶液压入装置Ⅱ的NaOH溶液中。
2.胶体的制备
(1)物理方法:研磨法。如制豆浆。
(2)化学方法:利用水解反应、复分解反应等。
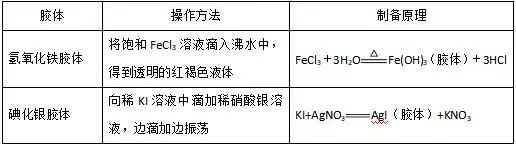
注意:
①制备氢氧化铁胶体时,不能搅拌也不能加热时间过长,否则会导致胶体聚沉。
②书写制备胶体的化学方程式时,用“=”,不用“?”,而且不能写“↓”符号。
3.检验Fe2+、Fe3+的常用方法
(1)根据溶液颜色:含有Fe2+的溶液显浅绿色,含有Fe3+的溶液显棕黄色。
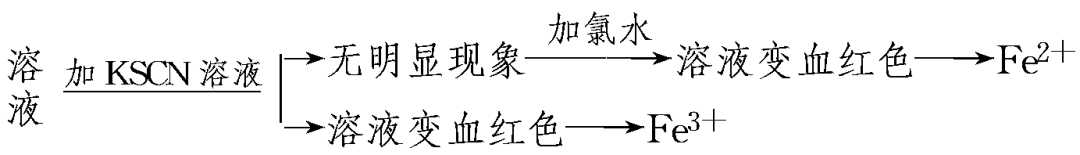
(2)用KSCN溶液和氯水
①流程:
(3)用NaOH溶液
①流程:
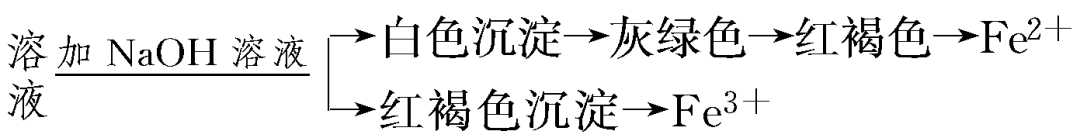
②有关反应:Fe3++3OH-===Fe(OH)3↓(红褐色沉淀)
Fe2++2OH-===Fe(OH)2↓(白色沉淀)
4Fe(OH)2+O2+2H2O===4Fe(OH)3

氢氧化铁胶体的制备:向沸水中逐滴加入FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制得Fe(OH)3胶体,化学方程式为FeCl3+3H2O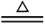 Fe(OH)3(胶体)+3HCl。
Fe(OH)3(胶体)+3HCl。
赞赏
长按二维码向我转账

受苹果公司新规定影响,微信 iOS 版的赞赏功能被关闭,可通过二维码转账支持公众号。
相关文章
推荐内容
学习方法
 平凉:职业教育搭平台
平凉:职业教育搭平台 习总书记关切事丨这一年
习总书记关切事丨这一年 国外创投新闻 印度教育
国外创投新闻 印度教育